Illustration of a healthy neuron (left), neuron with Alzheimer’s (center), and a dead neuron being engulfed by microglia (right). (Science Photo Library/Canva Pro) /Иллюстрация здорового нейрона (слева), нейрона с болезнью Альцгеймера (в центре) и мертвого нейрона, поглощенного микроглией (справа). ((Научная фотобиблиотека/Canvas Pro)
Ключ к предотвращению болезни Альцгеймера (Alzheimer’s) может быть у женщины, у которой никогда не было этого заболевания.
Несмотря на высокий генетический риск, женщина, носительница двух копий редкого генетического варианта, связанного с поздним началом болезни Alzheimer’s, называемого APOE3 Крайстчерч, оказалась устойчивой к когнитивному снижению при этом заболевании.
Теперь ученые наблюдали, как мыши с аналогичным набором генетических мутаций (microglia) реагировали на состояния, похожие на болезнь Альцгеймера.
Как и в случае с человеком, у мышей, по-видимому, было меньше неврологических дефектов, связанных с запущенными стадиями заболевания, причем ключевым фактором было то, как очищающие клетки мозга (микроглия) реагируют на патологию заболевания. Это дает новую надежду на разработку методов лечения болезни Альцгеймера, направленных на выявление именно этих реакций.
Исследовательская группа из медицинской школы Вашингтонского университета говорит, что этот ответ помогает разорвать связь между ранней, бессимптомной стадией болезни Альцгеймера и поздней стадией снижения когнитивных функций.
Как генетическая, называемая аутосомно–доминантной болезнью Альцгеймера (ADAD), так и негенетическая формы болезни Альцгеймера развиваются около 30 лет. Первые 20 лет или около того симптомы отсутствуют, поскольку амилоид накапливается в мозге медленно.
Когда уровень амилоида в мозге достигает критической точки, несколько разрушительных процессов начинают работать сообща. Белок под названием тау начинает скручиваться и распространяться, замедляя метаболизм мозга и вызывая сокращение тканей, что приводит к снижению когнитивных способностей.
«Один из самых больших вопросов, на которые нет ответа в области болезни Альцгеймера, заключается в том, почему накопление амилоида приводит к патологии тау», — говорит невролог Дэвид Хольцман.
«Любой защитный фактор очень интересен, потому что он дает нам новые ключи к пониманию того, как работает болезнь».
Одна большая семья в Колумбии имела дело с ADAD на протяжении многих поколений, причем симптомы начинались у половины членов семьи в возрасте за 40. В случае этой семьи заболевание было спровоцировано мутацией в гене под названием presenilin-1, связанной с повышенной склонностью к образованию амилоидных бляшек, причем накопление амилоида начинается примерно в возрасте 20 лет (amyloid plaques).
Одна особа в этой семье добилась того, что казалось невозможным: она оставалась когнитивно здоровой до 70 лет, несмотря на то, что унаследовала мутацию presenilin-1.
Женщина, по-видимому, была единственной в группе, у кого было две копии APOE3 Christchurch (APOE3ch), что было предложено в качестве объяснения ее удачи. У тех, кто нес только одну копию APOE3ch, все еще проявлялись признаки ухудшения когнитивных функций в более молодом возрасте.
Исследование, проведенное в 2019 году (A study in 2019 speculated), предположило, что дополнительные мутации у женщины задерживали процесс, замедляя быстрое распространение тау.
«Эта женщина была очень, очень необычной в том смысле, что у нее была патология амилоида, но не сильно выраженная тау-патология и только очень слабые когнитивные симптомы, которые проявились поздно», — объясняет Хольцман. «Это навело нас на мысль, что у нее могут быть ключи к разгадке связи между амилоидом и тау».
Но поскольку этот специфический набор генетических мутаций был зарегистрирован только у одного человека в мире, было невозможно определить, могут ли другие факторы быть вовлечены в ее замечательное когнитивное здоровье.
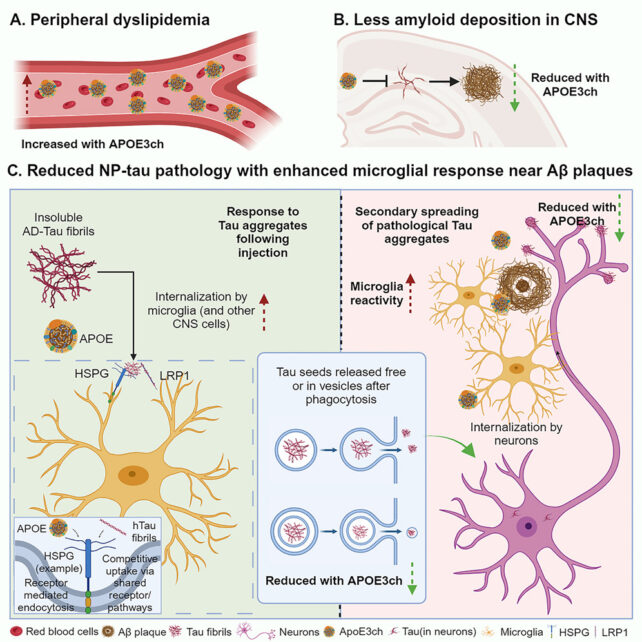
Graphical depiction of how the APOE3ch genes altered pathology in mice. Graphical depiction of how the APOE3ch genes altered pathology in mice. (Chen et al., Cell, 2023)/Графическое изображение того, как гены APOE3ch изменяли патологию у мышей. Графическое изображение того, как гены APOE3ch изменяли патологию у мышей. (Chen et al., Cell, 2023)
Итак, Хольцман и его коллеги изучали мышей, которые были генетически модифицированы для выработки избытка амилоида, и ввели ген с мутацией APOE3ch. Затем они ввели небольшое количество тау, которое, как ожидалось, вызовет проблемы в мозге, уже заполненном амилоидом.
В мышиных моделях, как и в случае с колумбийкой, тау-белок распространялся не так, как ожидалось. Причина: микроглия вокруг амилоидных бляшек была суперактивна и эффективно очищала белок.
«Эти микроглии поглощают тау и разрушают его, прежде чем тау-патология сможет эффективно распространиться на следующую клетку», — говорит Хольцман.
«Это заблокировало большую часть последующего процесса; без тау-патологии у вас не будет нейродегенерации, атрофии и когнитивных проблем».
Однако защитные эффекты APOE3ch при поздней стадии болезни Альцгеймера неясны и могут варьироваться в зависимости от происхождения человека или наличия других генетических мутаций. Это важная область, требующая дальнейшего изучения, добавляет команда.
«Если мы сможем найти способ имитировать эффекты мутации APOE в Крайстчерче, — says Хольцман, — возможно, нам удастся остановить людей, которые уже находятся на пути к деменции Альцгеймера, от продолжения этого пути».
Исследование было опубликовано в журнале Cell.
Автор: Rebecca Dyer
Источник: https://www.sciencealert.com/woman-who-defied-alzheimers-could-show-us-how-to-avoid-it
фото: Kampus Production
